
-
 06 June 2013
Алгебра
06 June 2013
Алгебра
- Автор: PAPA7
к раствору силиката калия массой 20,53 грамма и массовой долью 15% прилииизбыток раствора нитратата кальция. вычислить массы образовавшегося осадка
-
-

-
 06 June 2013
06 June 2013
- Ответ оставил: Чупокабр
K2SiO3+Ca(NO3)2=CaSiO3+2KNO3
1)m(K2SiO3)=w(K2SiO3)*m(раствора)=0.15*20.53=3.08
2)n(K2SiO3)=m(K2SiO3)/M(K2SiO3)=3.08/154=0.02
3)n(K2SiO3)=n(CaSiO3)=0.02
4) m(CaSiO3)=M(CaSiO3)*n(CaSiO3)=116*0.02=2.32
-
-

-
 06 June 2013
06 June 2013
- Ответ оставил: 2449Алия
K₂SiO₃ + Ca(NO₃)₂ = CaSiO₃ + 2KNO₃
Поскольку нитрат кальция нам дан в избытке, то K₂SiO₃ прореагирует полностью.
1) Найдем массу чистого (без примесей) K₂SiO₃:
20,53 г - это 100%
х г - это 15%
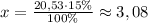 г K₂SiO₃
г K₂SiO₃M(K₂SiO₃)= 154 г/моль
M(CaSiO₃)= 116 г/моль
m(K₂SiO₃)= 3,08 г
m(CaSiO₃)= y г
2) Через расчет по уравнению реакции найдем массу образовавшегося осадка (CaSiO₃).
154 г K₂SiO₃ дают 116 г CaSiO₃
3,08 г K₂SiO₃ дают у г CaSiO₃
г CaSiO₃
Ответ: масса образовавшегося осадка равна 2,32 г.
-
-

- НЕ НАШЛИ ОТВЕТ?
Если вас не устраивает ответ или его нет, то попробуйте воспользоваться поиском на сайте и найти похожие ответы по предмету школьной программы: алгебра.
На сегодняшний день (29.04.2026) наш сайт содержит 449111 вопросов, по теме: алгебра. Возможно среди них вы найдете подходящий ответ на свой вопрос. -
Нажимая на кнопку "Ответить на вопрос", я даю согласие на обработку персональных данных
Ответить на вопрос



